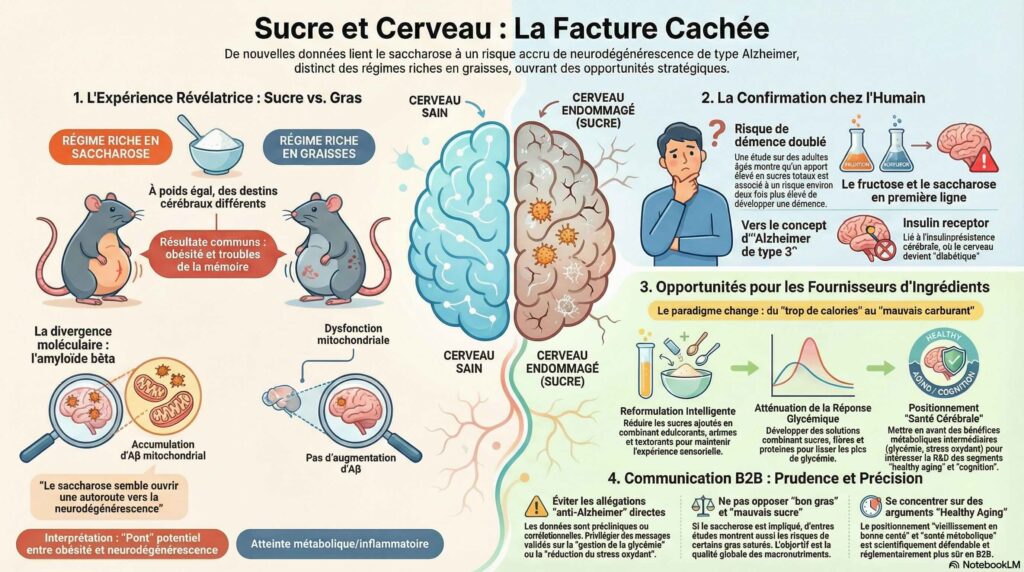
Même poids sur la balance, pas même destin pour le cerveau. C’est la conclusion contre-intuitive d’une étude mexicaine comparant deux régimes hypercaloriques chez le rat : sucre contre gras. Les deux groupes grossissent pareil, perdent la mémoire pareil — mais seul le groupe saccharose accumule de l’amyloïde bêta dans ses mitochondries cérébrales. La signature moléculaire d’Alzheimer, en somme. Le gras fait déborder la ceinture ; le sucre, lui, semble ouvrir un raccourci direct vers la neurodégénérescence.
Le sucre n’attaque plus seulement la ceinture
On pensait avoir compris l’équation : trop de sucre = obésité = diabète = problèmes. Simple, linéaire, presque rassurant dans sa prévisibilité. Les dernières données scientifiques viennent compliquer ce schéma confortable.
Une équipe mexicaine a comparé deux régimes hypercaloriques chez le rat : l’un riche en saccharose, l’autre en graisses. Résultat attendu : les deux groupes deviennent obèses, développent un syndrome métabolique et présentent des troubles de la mémoire. Résultat inattendu : seul le groupe « sucre » accumule de l’amyloïde bêta dans les mitochondries cérébrales — la signature pathologique de la maladie d’Alzheimer.
Autrement dit, à obésité égale, le saccharose semble ouvrir une autoroute vers la neurodégénérescence que le gras ne prend pas.
Sucre vs gras : deux routes, deux destinations cérébrales
Les chercheurs ont nourri des rats pendant plusieurs mois avec trois régimes distincts : standard, enrichi en saccharose, ou enrichi en graisses. Les deux régimes hypercaloriques conduisent à une obésité abdominale comparable, un dérèglement du métabolisme glucidique et un déclin mesurable de la mémoire spatiale.
La divergence apparaît au niveau moléculaire. Dans l’hippocampe et le cortex des rats « sucre », l’amyloïde bêta s’accumule dans les mitochondries — ces centrales énergétiques cellulaires deviennent des dépotoirs de protéines pathologiques. Le groupe « gras » ? Dysfonction mitochondriale aussi, mais pas d’amyloïde.
Les auteurs proposent que le saccharose crée un « pont » spécifique entre obésité et neurodégénérescence, via le stress oxydant et le dérèglement de l’amyloïdogenèse. Le gras fait grossir et fatigue le métabolisme ; le sucre fait ça plus quelque chose de spécifiquement neurotoxique.
Tableau — Sucre vs gras : deux profils de dommages
| Dimension | Régime riche en sucres (saccharose) | Régime riche en graisses |
| Effet sur le poids | Obésité abdominale et syndrome métabolique | Obésité abdominale comparable |
| Mémoire spatiale (rats) | Déclin significatif | Déclin similaire |
| Stress oxydant / mitochondries | Dysfonction + accumulation d’Aβ | Dysfonction sans excès d’Aβ |
| Marqueurs de type Alzheimer | Aβ mitochondrial élevé (hippocampe, cortex) | Pas d’augmentation d’Aβ |
| Interprétation | « Pont » potentiel obésité → neurodégénérescence | Atteinte métabolique/inflammatoire |
Les cohortes humaines confirment le signal
Les données animales ne restent pas isolées. Une étude sur des adultes âgés montre qu’un apport élevé en sucres totaux est associé à un risque environ doublé de développer une démence au cours du suivi — indépendamment du statut APOE ε4, de l’activité physique ou de la qualité globale du régime.
Dans les analyses par type de sucre, les participants dans le quintile le plus élevé de consommation de fructose et de saccharose présentaient un sur-risque significatif par rapport au quintile le plus bas. Une autre étude focalisée sur les femmes suggère une vulnérabilité particulière du cerveau féminin à l’excès de sucres — cohérent avec les observations sur d’autres pathologies métaboliques.
Ces données humaines renforcent le concept d' »Alzheimer de type 3″ : une forme de neurodégénérescence liée à l’insulinorésistance cérébrale, où le cerveau devient littéralement « diabétique » avant même que la glycémie périphérique ne déraille.
Ce que ça change pour les fournisseurs d’ingrédients
Le récit scientifique se déplace. On ne parle plus seulement de « trop de calories » mais de « mauvais carburant pour le cerveau« . Pour les fournisseurs d’ingrédients sucrants, cette évolution crée une pression supplémentaire — mais aussi des opportunités de différenciation.
- Reformulation intelligente. Réduire les sucres ajoutés et sucres libres tout en maintenant l’expérience sensorielle. Les solutions combinant édulcorants de haute pureté, arômes et texturants deviennent stratégiques.
- Atténuation de la réponse glycémique. Combinaisons sucres/fibres/protéines capables de lisser les pics de glycémie et, potentiellement, les dérives métaboliques associées aux sucres rapides.
- Positionnement « santé cérébrale ». Dans les limites réglementaires, mettre en avant des bénéfices métaboliques intermédiaires (glycémie, insulinosensibilité, stress oxydant) qui intéressent la R&D des clients industriels sur les segments healthy aging et cognition.
R&D : trois leviers concrets pour les portefeuilles sucrants
Explorer les alternatives au saccharose/fructose rapides. Sucres à libération lente, polyols ciblés, édulcorants intenses nouvelle génération, sucres rares. Le critère n’est plus seulement « moins sucré » mais « moins glycémique, moins pro-oxydant ».
Travailler sur les matrices. Fibres solubles, protéines, lipides structurés qui modulent la cinétique d’absorption. L’objectif : transformer un sucre « rapide » en sucre « lent » par effet de matrice.
FAQ : sucres, cerveau et démence
Peut-on parler de « sucres neurotoxiques » en B2B ? Avec prudence. Les modèles animaux montrent des lésions de type Alzheimer spécifiques au saccharose, et les cohortes humaines confirment l’association sucres/démence. Mais il s’agit de corrélations et de données précliniques — pas de preuves causales définitives. Restez sur des messages métaboliques (« gestion de la glycémie », « réduction du stress oxydant ») plutôt que des claims anti-Alzheimer.
Les graisses sont-elles « moins dangereuses » pour le cerveau ? Dans cette étude, oui — le gras n’induit pas l’accumulation d’amyloïde observée avec le sucre. Mais d’autres travaux montrent que certains profils lipidiques (graisses saturées notamment) sont aussi associés au déclin cognitif. Il ne s’agit pas d’opposer « bon gras » et « mauvais sucre », mais de travailler sur la qualité globale des macronutriments.
Faut-il intégrer la « démence » dans les argumentaires santé ? En B2B, le positionnement « healthy aging » et « santé métabolique » est défendable, en s’appuyant sur la littérature liant charge glucidique et insulinorésistance. Les claims explicites de réduction du risque d’Alzheimer nécessiteront encore des confirmations cliniques interventionnelles avant d’être réglementairement tenables.
Quels ingrédients sont les plus prometteurs ? Édulcorants permettant une réduction forte des sucres ajoutés, solutions de « sugar-stepping » progressif, combinaisons fibres/protéines pour atténuer la charge glycémique. Les dossiers incluant des marqueurs métaboliques avancés seront les plus convaincants pour les grands donneurs d’ordres.
En résumé
Références
- High-sugar diets may mimic Alzheimer’s pathology more closely than high-fat diets, PsyPost, 2025. PsyPost
- Sucrose-rich diet and mitochondrial amyloid-beta accumulation, PubMed, 2025. PubMed
- Sugar intake and incident dementia in older adults, Journal of Alzheimer’s Disease, 2023. SAGE Journals
- Dietary sugar and cognitive decline, PMC, 2024. PMC
